研究揭示压力助力免疫逃逸机制
美国纽约大学医学院Bossowski等研究发现,在缺氧、营养匮乏和代谢废物积累等不利环境压力下,肿瘤细胞会激活整合应激反应,导致调节代谢适应、存活和生长等转录程序的激活转录因子4(ATF4)上调,进而促进肿瘤细胞分泌脂质运载蛋白2(LCN2),通过促进免疫抑制性巨噬细胞的浸润来削弱抗肿瘤免疫。(Nature. 2026年2月18日在线版)
研究发现,在肺癌和胰腺癌患者中,LCN2与患者肿瘤内T细胞浸润减少相关;而抗LCN2抗体在侵袭性实体瘤小鼠模型中,可促进强烈的抗肿瘤T细胞反应,提示靶向LCN2是一种潜在的抗肿瘤免疫疗法。
已有研究发现,肿瘤细胞可通过激活整合应激反应,以适应外界环境压力并抵抗治疗。整合应激反应相关信号会汇集于激活转录因子4(ATF4),ATF4在肿瘤进展中究竟发挥什么作用有待探讨。
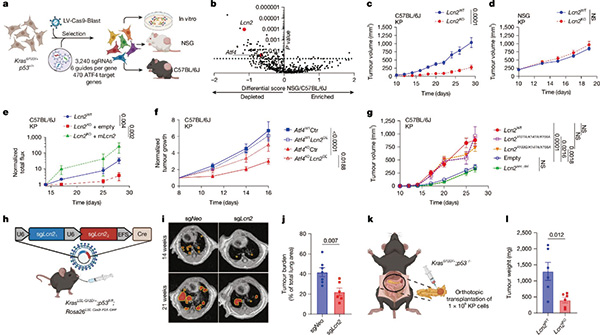
在免疫正常的肺癌小鼠模型中,研究者发现ATF4是肿瘤生长所必需的;但在免疫缺陷的裸鼠模型中,ATF4的缺失对肿瘤生长无影响,提示ATF4可能是通过抑制抗肿瘤免疫发挥促肿瘤作用。
研究者采用CRISPR-Cas9基因编辑技术筛选由ATF4驱动的免疫抑制因子,与炎症反应有关的分泌型糖蛋白——LCN2浮出水面。ATF4驱动的免疫逃逸,是通过LCN2实现的。
除了肺癌之外,LCN2对黑色素瘤和胰腺癌的生长也至关重要。在已形成的肿瘤中沉默LCN2,可显著抑制肿瘤生长,延长小鼠生存期并降低肿瘤负荷,提示LCN2是晚期肿瘤的治疗靶点。后续研究揭示了肿瘤细胞激活整合应激反应上调ATF4抑制抗肿瘤免疫的机制。
上调表达的ATF4会直接结合在LCN2编码基因的启动子区域,驱动这种分泌型糖蛋白的表达。分泌到肿瘤微环境中的LCN2通过与间质巨噬细胞上的SLC22A17结合,重塑巨噬细胞的转录状态,导致巨噬细胞中CXCL9(一种关键的T细胞趋化因子)的表达下降,同时增加促炎因子IL-6的表达,从而形成一个不利于免疫应答的炎症环境。
由于CXCL9水平降低,抗肿瘤的T细胞无法有效地募集并渗透进肿瘤内部。肿瘤细胞分泌的LCN2还与肿瘤内调节性T细胞的积聚呈正相关,这些细胞会进一步抑制效应T细胞的活性。
研究者在分析肺癌和胰腺癌患者肿瘤组织后发现,LCN2的表达水平与肿瘤分级、T细胞浸润减少、总生存期缩短及对免疫治疗反应差呈正相关。LCN2高表达与总生存期显著缩短相关。在一个肺癌队列中,LCN2低表达组的中位生存期为79个月,而LCN2高表达组的中位生存期为52个月。
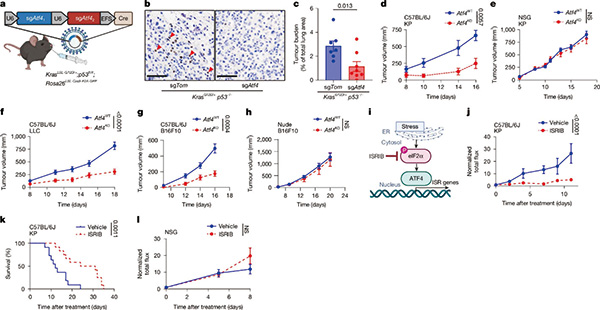
在确定LCN2与癌症进展密切相关之后,研究者合成了抗LCN2抗体,并证实这个抗体有抗肿瘤活性,且能延长肿瘤小鼠的生存时间。抗LCN2抗体能使对免疫治疗耐药的肿瘤恢复敏感性。在对PD-1抑制剂完全不响应的肺癌模型中,将抗LCN2抗体与PD-1抑制剂联合使用,效果优于单一疗法。
从肿瘤微环境来看,抗LCN2抗体治疗后,原本缺乏免疫细胞浸润的冷肿瘤内部出现了大量的效应T细胞,且瘤内巨噬细胞从免疫抑制状态转变为抗肿瘤状态(如降低IL-6水平,增加IFNγ浓度)。
该研究阐明了细胞压力感应与免疫逃逸之间的分子联系,并提出了一种极具潜力的新型联合免疫治疗策略,有望为肺癌和胰腺癌等肿瘤的治疗开启新研究路径。
(编译 王浩竹)














