研究揭示衰老促肺癌转移机制
瑞典哥德堡大学Patel等研究发现,衰老会重编程肺癌的演化轨迹,通过表观遗传激活整合应激反应(ISR),一方面限制原发肿瘤的生长,另一方面通过表观遗传途径激活了整合应激反应,赋予了肿瘤细胞致命的转移能力。衰老从根本上改变了肿瘤的发展方式,研究对衰老促进肿瘤转移的机制进行了探讨。(Nature. 2026年3月11日在线版)
探讨肿瘤机制的体内研究中,现有肺癌基因工程小鼠模型实验,几乎均在年轻小鼠(通常2~3个月龄)中进行,而临床实践中,非小细胞肺癌患者的诊断中位年轻高达70岁,发病年龄高峰在65~75岁。这种实验模型与真实世界患者群体在年龄维度上的严重脱节,或是许多临床前研究中表现优异的靶向疗法,在人体临床试验中遭遇失败的原因之一。
为对此进行探讨,研究者分别在2~3月龄和18~19月龄经典KP小鼠模型(携带 Kras-G12D 突变且 Trp53 基因敲除)肺部,通过气管内滴注含有 Cre 重组酶的病毒颗粒,同步诱发肺部肿瘤,分别代表青年期和老年期肺癌模型。在该体系中,18~19个月大老龄小鼠在经历5~6个月肿瘤发展期后,其生理年龄恰对应人类70岁左右,完美复刻人类非小细胞肺癌最典型的高发受众群体特征。
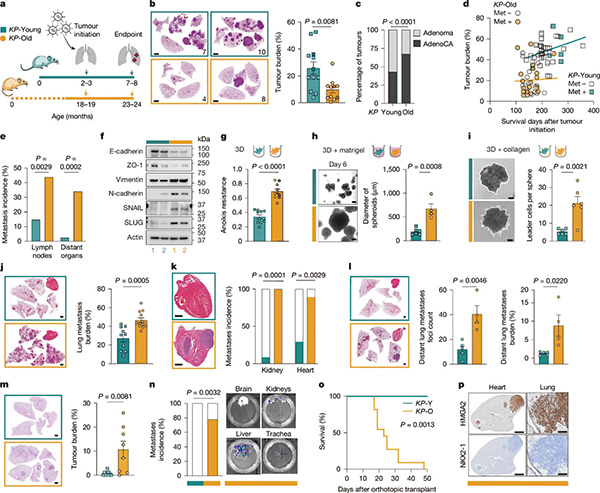
与青年期小鼠模型相比,老年期小鼠模型的原发性肺肿瘤负荷降低2.5倍;且不仅仅是负荷低,还表现出肿瘤数量更少、体积更小、增殖标志物(如磷酸化组蛋白 H3)的表达水平更低,但恶性程度更高的特征。在特定的观察窗口期,青年期小鼠模型原发性肺肿瘤负荷随时间呈线性增加;老年期小鼠的肿瘤负荷保持较低水平,但却极早地出现了局部淋巴结和远端器官的转移,并伴随着总生存期的急剧缩短。
研究者分别从两个小鼠模型体内分离癌细胞在体外培养,探讨老年期小鼠那较小且生长较慢的原发性肺肿瘤,为何会更快地进展为转移性肺癌。体外培养结果显示,老年期小鼠体内的肿瘤细胞有些不寻常的特征:上皮-间质转化标志物的表达增加,对失巢凋亡的抵抗力增加,提示衰老或赋予了肿瘤细胞更强的转移能力。生理性的衰老过程在细胞内源性层面重塑了肺癌细胞,限制了它们在原位的高速增殖,却为其换取了挣脱原位微环境束缚、进行远端器官播散与定植的致命特权。
在衰老的肿瘤细胞中,表观遗传修饰发生了改变。作为整合应激反应的核心效应因子,调节代谢适应、存活和生长等转录程序的激活转录因子4(ATF4)编码基因的染色质开放程度增加。这种染色质状态的变化,导致衰老细胞对应激(如营养匮乏)更加敏感,使ATF4信号能持续且高水平激活,不像年轻细胞那样能迅速恢复平衡。
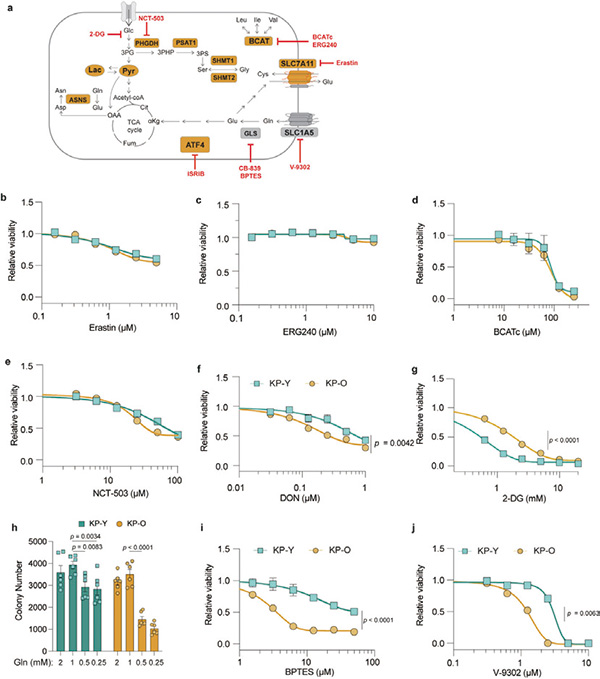
ATF4能驱动肿瘤细胞的上皮和谱系可塑性。研究发现,ATF4表达与上皮-间质转化标志物的增加直接相关,增强了肿瘤细胞的侵袭能力。ATF4还会提升肿瘤细胞在脱离原发灶后的生存能力,即失巢凋亡抗性,这是肿瘤细胞实现远端扩散的关键特征。研究证实,在年轻细胞中过表达ATF4足以诱导转移,而抑制衰老细胞中的ATF4则能阻断转移。ATF4还会重编程肿瘤细胞的代谢模式,使其从依赖葡萄糖转向依赖谷氨酰胺代谢(谷氨酰胺分解),这种代谢灵活性为转移过程提供了必要的能量支持。
研究者分析临床数据后发现,ATF4在老年肺癌患者的肿瘤中显著富集,且ATF4高表达与更晚的分期、较差的生存率和更高的复发风险密切相关。提示衰老-ATF4轴可能是老年患者非小细胞肺癌转移的关键驱动因素。
该研究揭示,衰老会促使肿瘤“劫持”整合应激反应通路,使肿瘤细胞能重新编程其新陈代谢;这种代谢重编程虽不会让肿瘤生长得更快,但会提升肿瘤细胞转移能力。这一发现让我们对老年肺癌有了新认知,不仅解释了为何肺癌在老年患者中更具侵袭性,也为老年肿瘤患者的治疗提供了新启示。 (编译 王浩竹)














