国人研究设计“双面胶”助力CAR-T疗法
中国科学院过程工程研究所魏炜和马光辉、南方医科大学珠江医院李玉华、中国医学科学院血液病医院王建祥联合研究团队,在临床研究中发现,白血病细胞和CAR-T细胞均特异性高表达CD71蛋白,基于CD71的天然配体铁蛋白,创造性设计了一个名为铁蛋白团簇细胞连接子(FACE)球状大分子。(Cell. 2026年3月9日在线版)
实验结果显示,表面粘满FACE的CAR-T细胞进入身体后,对白血病细胞的识别和杀伤变得更强;无论输注CAR-T细胞的剂量较低,还是白血病细胞表面抗原密度降至正常值10%以下,均可发挥很好的抗癌作用。研究者尝试在FACE这个球状大分子中塞入化疗药物,发现可进一步提升抗癌效果。
研究者此前即注意到,不同类型白血病患者的癌细胞均高表达CD71。研究者设计了基于铁蛋白的砷靶向递送系统,可将砷输送至多种类型的白血病细胞,从而产生强大的抗白血病治疗效果。
该研究发现,不仅白血病细胞高表达CD71,用于治疗白血病的CAR-T细胞也高表达CD71,于是研究者想到利用CD71的天然配体铁蛋白,将二者连在一起。考虑到单个铁蛋白分子太小,在与CAR-T细胞的CD71结合之后,会被内吞。研究者将多个铁蛋白交联成粒径约为600 nm的球状FACE分子,超过了T细胞的内吞阈值,能稳定地锚定在CAR-T细胞表面,每个细胞最多约能结合250个FACE颗粒。
FACE 上的多个铁蛋白单元可以同时结合 CAR-T 细胞和白血病细胞表面的 CD71,显著增强两者间的物理相互作用力。这种强力的“拉近”效应,极大地增加了 CAR-T 细胞表面 CAR 与癌细胞上残存靶抗原的接触机会。即使癌细胞因抗原调变导致抗原密度很低,FACE 也能帮助 CAR-T 细胞成功激活,相当于降低了 CAR-T 细胞的“启动阈值”。
体外实验数据显示,FACE使CAR-T细胞与患者来源白血病细胞之间的相互作用力最高提升了24.6倍;FACE-CAR-T细胞的增殖速度约快2倍,72小时增殖率达88.6%;颗粒酶B和干扰素γ的阳性百分比分别提升了1.7倍和3.3倍;即使在效靶比极低或白血病细胞抗原表达下调的情况下,FACE-CAR-T细胞的杀伤率仍比普通CAR-T细胞高出至少一倍。
从患者来源的异种移植模型来看,即使在输注剂量只有标准剂量五分之一的情况下,FACE-CAR-T细胞仍可达到标准剂量常规CAR-T细胞的清除效果,并在第30天完全根除外周血中的白血病细胞。在常规CAR-T细胞疗效不佳的CD19低表达模型中,FACE-CAR-T细胞仍能有效消除肿瘤,让小鼠在60天内100%存活。
在安全性方面,相比高剂量常规CAR-T细胞,低剂量FACE-CAR-T细胞产生的炎症细胞因子水平更低;此外,FACE-CAR-T细胞治疗组小鼠体重保持稳定,也未观察到脱靶毒性。问题来了,既然白血病细胞和CAR-T细胞都表达CD71分子,那输注到体内的FACE-CAR-T细胞会不会聚集在一起,并带来安全性问题。
研究者通过流式细胞术检测了FACE-CAR-T细胞在体内的分散状态。结果显示,在注入小鼠体内24小时后,FACE-CAR-T细胞在血液中主要以单细胞形式存在,FACE-CAR-T细胞的单细胞百分比与常规CAR-T细胞相当(分别为99.71%和97.93%),两者之间无显著性差异。
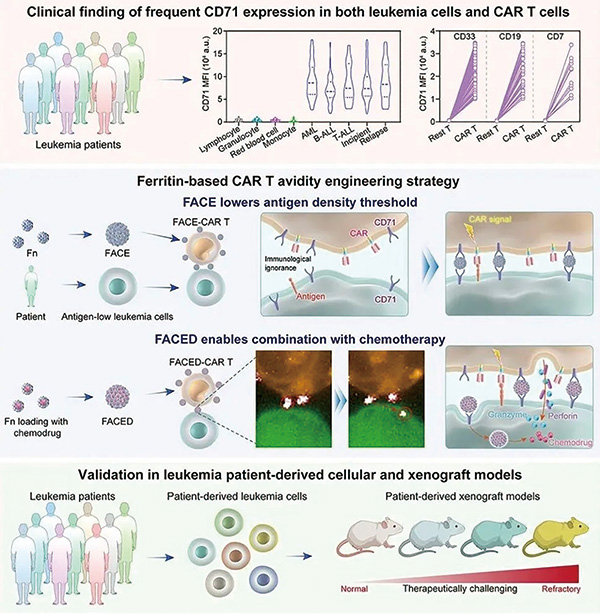
考虑到癌细胞表面抗原表达下调或者直接丢失的问题,对于靶抗原丢失,仅靠将CAR-T和癌细胞粘在一起是没用的。研究者利用铁蛋白内部固有笼型空腔结构,将 FACE 升级为 FACED,成功将临床上常用的化疗药物(例如三氧化二砷、长春新碱、柔红霉素、阿糖胞苷等)装载进去,这样一来,FACED-CAR-T 细胞就变成了“双模式”杀手:既能通过 CAR 介导免疫杀伤,又能局部靶向释放化疗药物,对完全抗原阴性的癌细胞同样能产生疗效。
体内实验显示,FACE搭载化疗药物之后,在体内展现了双重功能:作为衔接器引导CAR-T识别癌细胞;被白血病细胞内吞后,可释放化疗药物杀伤癌细胞,从而有效应对靶抗原缺失引起的复发。
实时荧光成像显示,FACE最初定位于CAR-T细胞与白血病细胞的接触界面;随着时间推移,由于白血病细胞具有更高的CD71表达量和更强的细胞膜运动能力,FACE会从CAR-T细胞表面转移并被白血病细胞内吞,从而完成精准的药物递送,进而达到释放药物杀死癌细胞的目的。
研究者通过分析临床样本和CAR-T细胞的特征,发现CD71在白血病细胞和CAR-T细胞表面均特异性高表达,于是利用CD71的天然配体铁蛋白,巧妙地设计了一个“双面胶”,让CAR-T细胞可更好地识别并结合白血病细胞。通过创新性在“双面胶”中植入化疗药物,达到杀伤靶抗原低表达或不表达癌细胞的目的,尽可能防止癌症复发。 (编译 王浩竹)














