研究揭示三阴性乳腺癌免疫逃逸机制
美国丹娜-法伯癌症研究所Cassandras等研究发现,对于散播到肺部的三阴性乳腺癌细胞,糖皮质激素受体激活让其具备了免疫逃逸的能力。糖皮质激素受体抑制剂米非司酮或能助力防止转移。(Nature. 2026年3月4日在线版)
研究显示,糖皮质激素受体激活下调肿瘤细胞表面死亡受体FAS表达,阻止其与T细胞和NK细胞表面的FAS配体结合,避免触发肿瘤细胞的死亡程序。与慢性压力相关的糖皮质激素受体激活,不仅通过中性粒细胞改造肺部的免疫微环境,还赋予了散播肿瘤细胞免疫逃逸能力。
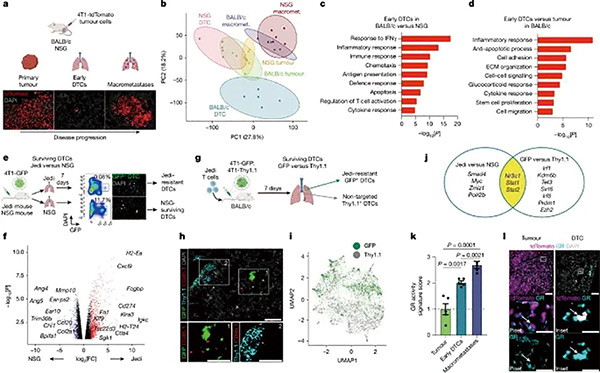
研究者此前一直在思考:肿瘤通过搭建免疫抑制微环境实现免疫逃逸,那脱离原发灶进入转移组织/器官的散播癌细胞是如何实现免疫逃逸的?为弄清这一问题,研究者将被绿色荧光蛋白(GFP)标记的三阴性乳腺癌细胞系(4T1),分别接种到免疫健全和免疫缺陷的小鼠体内,然后区分为原发灶、早期肺部散播癌细胞(DTC)和已形成转移灶阶段收集癌细胞,并对所有癌细胞展开转录组分析。
分析发现,免疫健全和免疫缺陷小鼠的DTC细胞转录组存在巨大差异。与免疫缺陷小鼠的DTC和免疫健全小鼠的原发灶癌细胞相比,免疫健全小鼠的DTC中免疫应答程序增强是主要变化,提示在转移播散阶段DTC确实面临免疫压力。
研究者构建了表达GFP的4T1癌细胞,小鼠体内的T细胞也很独特,是有GFP抗原特异性的CD8阳性T细胞。在这种小鼠体内,能存活下来的癌细胞,就是实现免疫逃逸的DTC。
在分离出从虎口逃脱的DTC后,研究者开展了转录组分析,这些实现免疫逃逸的DTC上调了与免疫逃逸有关的基因和与免疫应答相关的通路,说明它们确实遭遇了GFP抗原特异性的CD8阳性T细胞。
在分析免疫逃逸DTC上调的基因后,研究者发现,编码糖皮质激素受体的基因赫然在列。后续蛋白层面分析证实,实现免疫逃逸的DTC确实上调了糖皮质激素受体,而在免疫缺陷小鼠体内,DTC的糖皮质激素受体未出现上调,只在转移灶形成后才出现上调,这与之前的研究保持一致。
在后续研究中,研究者通过抑制糖皮质激素受体编码基因表达,证实糖皮质激素受体确实参与了散播到肺部癌细胞的免疫逃逸。用合成糖皮质激素地塞米松预处理4T1细胞激活糖皮质激素受体后,DTC的数量增加。糖皮质激素受体激活在结肠癌和黑色素瘤也有类似的促转移作用。糖皮质激素受体帮助DTC免遭CD8阳性T细胞和NK细胞的杀伤作用。
分子机制研究显示,DTC的糖皮质激素受体被激活后,会与死亡受体FAS编码基因的启动子结合,阻止FAS表达,降低DTC细胞表面的FAS水平;FAS减少就无法与CD8阳性T细胞和NK细胞的FAS配体结合,导致DTC体内的凋亡程序无法启动, DTC就逃避了免疫细胞的杀伤作用。
研究者测试了已获批上市的米非司酮,因其有抑制糖皮质激素受体激活的功能。在治疗三阴性乳腺癌小鼠模型时,虽然米非司酮、PD-1抑制剂及二者联合使用,均未能抑制原发灶的生长,但米非司酮减少了转移灶数量,联合PD-1抑制剂还能进一步降低转移负荷,延长小鼠的生存期。
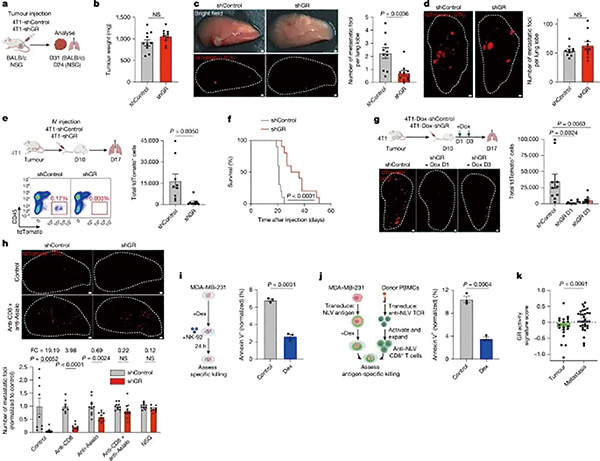
研究者在分析三阴性乳腺癌患者临床队列数据发现,与响应治疗的患者相比,治疗后疾病进展的患者糖皮质激素受体表达水平更高、激活特征增强,提示该研究发现的机制在人体内可能也存在。
该研究表明,糖皮质激素受体虽然对原发灶的影响微乎其微,但在保护DTC免遭免疫系统攻击方面发挥重要作用,是癌细胞转移复发的重要影响因素。期待研究结果尽早转化到临床应用,切实降低乳腺癌患者复发风险。米非司酮作为已上市40余年的老药,其安全性数据明确,与免疫治疗联合用于术后辅助治疗的可行性值得尽快开展临床研究验证。
(编译 王浩竹)














