早期肿瘤诱导周围成纤维细胞助力长期留存
英国剑桥大学Skrupskelyte等研究发现,新生肿瘤并非仅靠基因突变维持,而是通过应激反应诱导周围的成纤维细胞转化为支持性的“癌前生态位”,进而促进自身的长期留存。研究揭示了肿瘤与微环境在极早期阶段的互作机制,为阻断肿瘤早期进展提供了新的干预思路。(Nature. 2026年3月4日在线版)
为探讨癌前新生肿瘤持续存在的潜在机制,研究者采用了一种成熟的小鼠模型,用烟草烟雾中的一种诱变剂——二乙基亚硝胺(DEN),诱导小鼠模型的上消化道肿瘤发生。实验显示,出现肿瘤的时间最早为DEN处理后的第10天,这些新生肿瘤非常小,仅包含10个细胞。在短暂的形成期后是一个肿瘤清除过程,超过三分之一的初始肿瘤会逐渐被清除;存活的肿瘤虽可持续存在一年以上,但只有极少数能进展为恶性肿瘤。
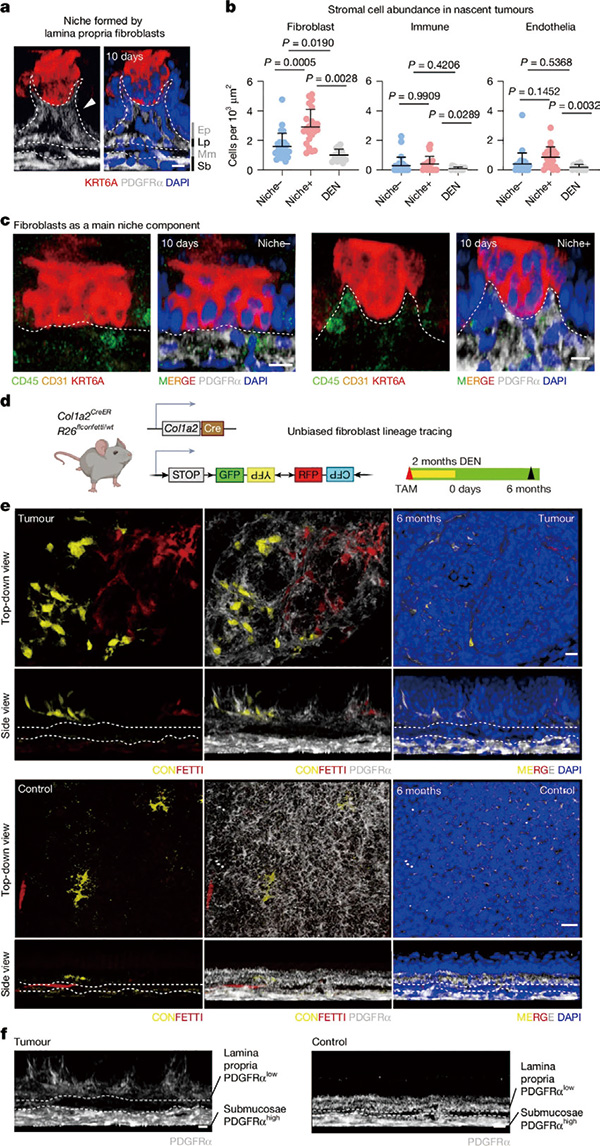
通过对比不同时间的肿瘤,研究者发现长期存留的肿瘤具有明显的基质重塑特征,表现为基质成纤维细胞围绕肿瘤形成了支持性的支架结构。若回到最早出现肿瘤那个时间点,约70%的新生肿瘤没有基质重塑特征。
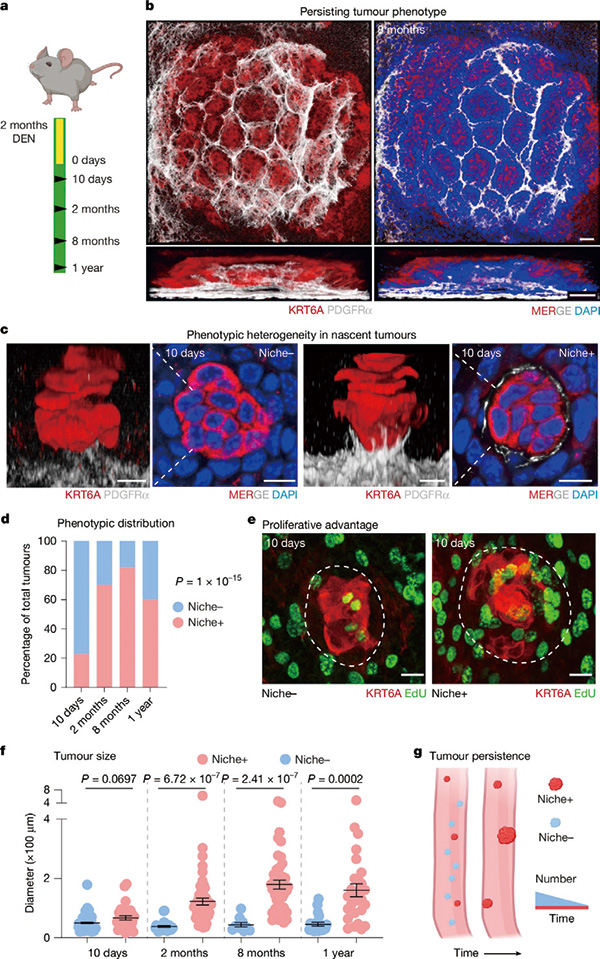
通过长时间的追踪观察,研究者发现,存在基质重塑的肿瘤数量保持恒定,而没有基质重塑的肿瘤逐渐减少。有基质重塑的肿瘤表现出更高的增殖活性,且更有可能持续存在并增大,提示基质重塑与新生肿瘤存活之间确实存在相关性。
为验证二者存在因果关系,研究者将从未接触过致癌物的健康上皮细胞放在肿瘤基质上培养,发现健康上皮竟获得了肿瘤样形态并高度增殖。这些接触过肿瘤基质的健康细胞,在移植到体内时也更容易实现长期植入,提示基质重塑是新生肿瘤生存的原因而非结果。后续研究明确PDGFRα低表达的成纤维细胞是基质重塑的主体。
从机制上看,在面对致癌物质压力的时候,不同空间位置的健康上皮细胞会发生不同的反应,其中一小部分上皮细胞会进入一种特殊应激状态,这种状态的特征是高表达SOX9转录因子,及通过旁分泌方式释放EGF配体。
这些配体作用于基质中PDGFRα低表达成纤维细胞表面的EGFR受体,驱动成纤维细胞向新生肿瘤部位迁移并发生空间重新排布,将新生肿瘤包裹起来形成支持性的结构。成纤维细胞还会大量分泌并沉积纤连蛋白(FN1),形成一个富含FN1的基质支架;这种富含FN1的支架通过与上皮细胞的整合素受体结合,反作用于上皮细胞,增强其增殖活性并赋予其肿瘤特性。
该研究表明,促癌物质处理后,一些上皮细胞应激激活转录因子SOX9,并释放EGF招募成纤维细胞,促使成纤维细胞大量分泌FN1,为新生肿瘤打造一个具有保护作用的温床,防止新生肿瘤被清除,最终促进新生肿瘤的生长和进展。这一发现加深了我们对肿瘤早期发展过程的认知,研究揭示的相关机制或可为癌症预防开辟新途径。 (编译 王浩竹)














