超敏CAR-T疗法破解低抗原密度难题
美国哥伦比亚大学Hanina等报告研究显示,肿瘤中CD70的异质性表达是通过表观遗传机制调控的,个体细胞中的表达范围从高到极低不等,尽管通过常规检测方法呈阴性状态。利用一种高度灵敏的CD70受体(即 HLA无关T细胞受体,该受体同时表达CD80和4-1BBL以提供共刺激作用),可有效消除逃避典型CAR-T细胞的CD70异质性肿瘤。(Science. 2026年2月26日在线版)
CD70属于肿瘤坏死因子超家族,正常组织中表达有限,在肾癌、卵巢癌、胰腺癌及胶质瘤中异常激活,是有潜力的免疫治疗靶点。此前研究显示,CD70在实体瘤中的表达通常较低,传统CD70-CAR-T仅能杀伤高表达细胞,难以完全清除肿瘤。
研究者发现,CD70在某些实体瘤中所有肿瘤细胞表面均表达,不过有些肿瘤细胞表达水平高,有些表达水平极低,此前未发现这一现象,是因为传统检测手段灵敏度不够,将极低表达当作不表达。研究发现,通过常规流式和免疫组化判定为CD70阴性的肾癌细胞,在高分辨率共聚焦显微成像下仍显示微弱但稳定的CD70信号。研究者采用一种突破光学衍射极限的超高分辨率荧光显微技术——受激发射损耗显微镜(STED),发现在CD70高表达和低表达的两种肾癌患者来源的异种移植瘤(PDX)模型中,分别至少有92.2%和82.5%的肿瘤细胞表达CD70。研究者推测,这些阴性肿瘤细胞并非不表达抗原,而是表达水平低到常规检测方法无法检测到。
为验证这一推测,研究者进行了系统实验,发现在肾癌、卵巢癌、胰腺癌模型中,CD70在肿瘤细胞上均有表达,只不过水平跨度极大,部分细胞低至常规检测下限,形成“假阴性”的伪异质性。接下来,设计能识别极低水平抗原,又不受HLA限制的通用型T细胞受体。传统CAR-T灵敏度不够,无法识别极低水平抗原,天然T细胞受体灵敏度比传统CAR高数十倍,但必须依赖HLA递送,HLA个体差异极大,难以开发通用型疗法。
研究者此前开发出一种超敏受体即非HLA依赖性T细胞受体(HIT),HIT受体识别癌细胞表面抗原的敏感性,远高于传统CAR。只要癌细胞表面有20个左右抗原分子,HIT受体就能识别,而传统CAR则至少需要肿瘤细胞表面有200个抗原才能识别并激活。
这种HIT受体保留CAR的抗原靶向可编程性,可直接识别细胞表面游离抗原,完全摆脱天然TCR的HLA限制,无需配型即可适用于所有患者。可使天然信号通路超敏放大,通过CRISPR基因编辑,将HIT受体定点敲入T细胞的内源TRAC位点,精准模拟天然TCR的α/β异源二聚体生理构象,直接劫持天然TCR-CD3复合体的下游信号通路,使受体对低密度CD70灵敏度提高10~50倍。其共刺激分子增强体内持久性,HIT-T共表达CD80和4-1BBL,提高T细胞活化、扩增和体内存续时间,有效减少微环境耗竭。
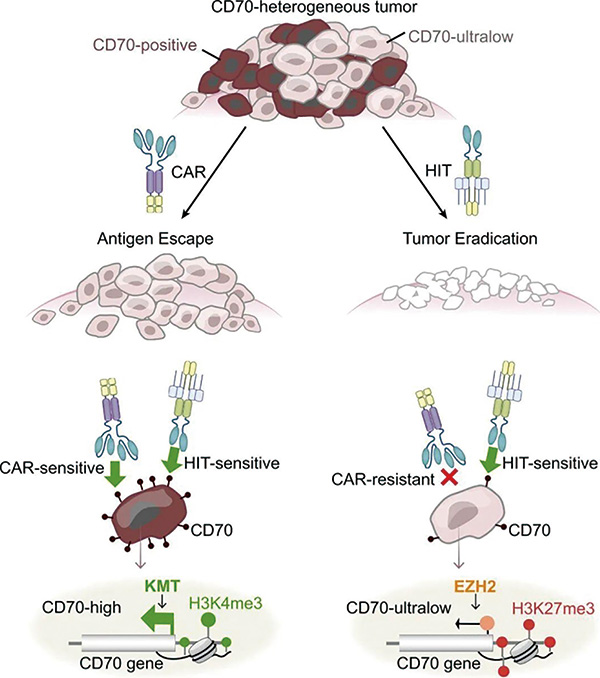
动物实验中,HIT-T显示出颠覆性疗效。在卵巢癌、胰腺癌小鼠模型及多线治疗耐药的转移性肾透明细胞癌PDX模型中,传统CD70-CAR-T仅能部分降低肿瘤负荷,而HIT-T细胞可完全且持久地清除肿瘤,使肿瘤负荷降至检测下限。靶向CD70并表达共刺激因子CD80和4-1BB配体的HIT-T细胞,在两种肾癌PDX模型中,均实现了完全且持久的肿瘤清除。靶向CD70的HIT-T细胞,也可清除胰腺和卵巢肿瘤。
基于血液系统肿瘤的研究表明,HIT-T细胞在控制低抗原丰度肿瘤方面的表现,显著优于传统的第一代和第二代CAR-T细胞。研究者在观察CD70高表达实体瘤时发现,它在多种实体瘤中异常高表达(70%~80%的肾癌和卵巢癌,25%的胰腺癌),而它的生理表达仅限于部分活化的免疫细胞亚群,因此成为极具吸引力的CAR-T细胞靶点。
这种降低免疫激活阈值的策略面临一个问题,那就是T细胞变得过于灵敏,会否攻击正常组织中微量表达的CD70,从而引发严重毒性反应。为评估这一风险,研究者进行了全组织筛查,整合覆盖30余种人体组织、222种细胞类型的单细胞转录组图谱,发现CD70在正常组织中的表达主要限于少量免疫细胞,且比例极低(<5%),CD70基因座在绝大多数成人正常组织中处于“关闭”状态,食管上皮细胞是唯一可能表达CD70的非免疫细胞类型(约3%的细胞),绝大多数重要器官(心、肺、肝、脑)几乎不表达。
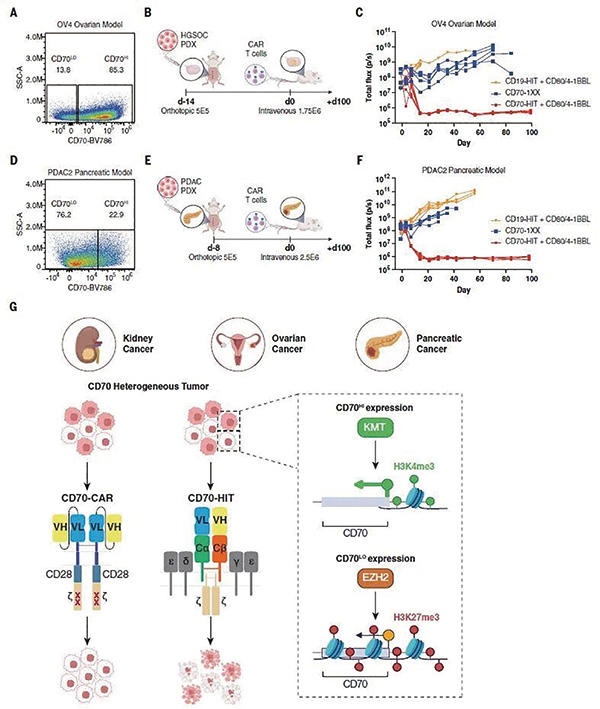
体外细胞毒性实验和体内人源化模型中,CD70-HIT表现出的毒性并未超过传统的CD70-CAR或CD19-CAR。该研究发现,某些实体瘤肿瘤细胞存在共同抗原靶点CD70,基于超敏的HIT受体技术开发了靶向CD70的超敏HIT-T细胞,在小鼠模型中实现了对肾癌、胰腺癌和卵巢癌的清除。有评论者指出,HIT-T概念极具突破性,向人体临床转化的技术难度不大,但须开展严格的临床试验并关注食管上皮潜在损伤。不过,该技术或为实体瘤治疗提供了新的技术路径。
(编译 王浩竹)














