HER2阳性乳腺癌和三阴性乳腺癌 ctDNA检测可指导治疗
美国华盛顿大学弗雷德·哈钦森癌症中心Hunter等报告的PREDICT研究结果显示,在人表皮生长因子受体2(HER2)阳性乳腺癌和三阴性乳腺癌(TNBC)患者中,新辅助治疗后的循环肿瘤DNA(ctDNA)不能区分病理完全缓解(pCR)与非pCR。然而,ctDNA提供了显著更优的预后分层,可识别出预后极佳和风险极高的患者。这些发现支持基于ctDNA指导的治疗降阶梯和升阶梯策略。(J Clin Oncol. 2026年3月10日在线版)
Ⅱ/Ⅲ期HER2阳性乳腺癌或TNBC患者常接受新辅助治疗。虽然pCR与改善的预后相关,但许多非pCR患者仍可长期生存。ctDNA微小残留病(MRD)评估可能提供额外的或更优的风险分层。
病理学疗效评估与ctDNA检测是一项前瞻性、多中心研究,采用基于肿瘤信息、超灵敏检测评估ctDNA作为治疗反应的生物标志物。主要目的是确定新辅助治疗后ctDNA对pCR的阴性预测值是否≥90%。针对TNBC队列的一个预设次要目的是评估ctDNA与5年无浸润性疾病生存期之间的相关性。研究分别在基线、新辅助治疗后手术前及手术后评估ctDNA。
在入组的227例患者中,220例可评估pCR(48%为HER2阳性乳腺癌;52%为TNBC),91例(41%)患者达到pCR。主要目标未达成。尽管所有pCR患者在新辅助治疗后ctDNA均为阴性,但40%的非pCR患者的ctDNA也为阴性(阴性预测值为60%)。
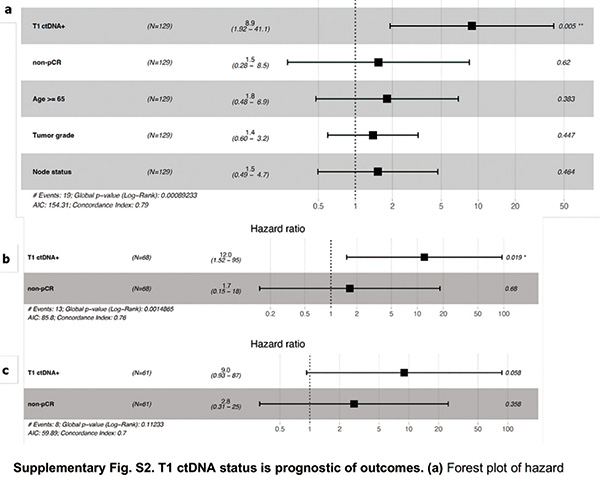
然而,预设的次要目标得以达成。新辅助治疗后检测到的ctDNA是复发的预后因素(HR=8.9,95%CI 2.4~33,P=0.001),且独立于pCR状态。此外,手术后检测到的ctDNA可识别出具有极高复发风险(HR=128,95%CI 15~1083,P<0.001)的患者,而手术后ctDNA阴性患者的5年无浸润性疾病生存率达94%。
(编译 郭晓丽)














