HER2阳性乳腺癌 基于MRI的新辅助周期个性化调整生存结局良好
荷兰癌症研究所Sonke等报告,在Ⅱ~Ⅲ期HER2阳性乳腺癌患者中,基于MRI引导的新辅助化疗周期优化策略与良好的3年无事件生存结局相关。这一方法代表了一种新的治疗策略,能够减轻部分早期HER2阳性乳腺癌患者的治疗负担、减少毒性并保持生活质量。(Lancet Oncol. 2026年2月16日在线版)
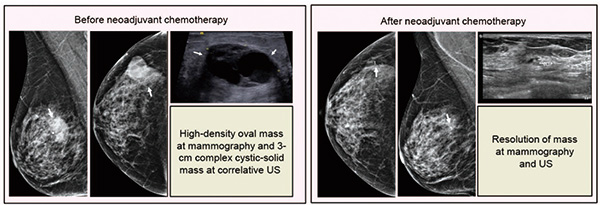
对于Ⅱ~Ⅲ期HER2阳性乳腺癌患者,包含6~9个周期抗HER2为基础的新辅助化疗可带来较高的病理完全缓解率和优异的生存结局,但也伴有显著的不良反应。TRAIN-3研究旨在探讨接受该方案治疗且在MRI上出现快速、完全影像学缓解的患者,是否适合提前进行手术。研究表明,激素受体阴性肿瘤患者中有三分之一,激素受体阳性肿瘤患者中有六分之一,在仅接受3个周期化疗后即获得病理完全缓解。在此报告主要终点,即3年无事件生存率的结果。
TRAIN-3是一项在荷兰43家医院进行的多中心、单臂、Ⅱ期研究。符合条件的患者为年龄≥18岁、WHO体能状态评分为0或1、确诊为Ⅱ~Ⅲ期的HER2阳性乳腺癌。患者接受的新辅助化疗方案包括:紫杉醇(每21天为一个周期,第1、8天静脉给药,80 mg/m2)、曲妥珠单抗(每周期的第1天静脉给药6 mg/kg,第一周期第1天负荷剂量为8 mg/kg)、卡铂(每周期的第1天静脉给药,AUC为每分钟6 mg/mL)和帕妥珠单抗(每周期的第1天静脉给药420 mg,第一周期第1天负荷剂量为840 mg),最多治疗9个周期。
一旦MRI观察到完全影像学缓解,即转诊进行手术。术后获得病理完全缓解的患者,完成1年的曲妥珠单抗和帕妥珠单抗辅助治疗。若切除标本中仍有残留浸润性病灶,则继续化疗直至完成总共9个周期,随后接受14个周期的T-DM1辅助治疗(每21天一周期,第1天静脉给药,3.6 mg/kg)。
研究记录3级或以上不良事件以及2级或以上的左心室射血分数和神经病变不良事件,直至最后一次辅助治疗结束后30天。主要终点是3年无事件生存率,分析按激素受体状态(阴性/阳性)分组,在意向治疗人群中进行。本研究患者招募已结束,次要终点的随访仍在进行中。
2019年4月1日至2021年5月12日,共入组了235例激素受体阴性肿瘤患者和232例激素受体阳性肿瘤患者。除1例外,所有参与者均为女性。中位随访时间为40.1个月(IQR:35.3~45.6个月)。激素受体阴性组患者的3年无事件生存率为92.2%(95%CI 88.7%~95.9%),激素受体阳性组的为92.0%(95%CI 88.5%~95.6%)。总共有40例(9%)患者发生了事件(激素受体阴性组19例,激素受体阳性组21例)。
在接受1~3个周期化疗的患者中,激素受体阴性组的3年无事件生存率为96.1%(95%CI 91.8%~100%),激素受体阳性组的为98.6%(95%CI 95.8%~100%)。接受4~6个周期化疗患者的无事件生存率分别为89.2%(95%CI 82.4%~96.6%)和94.2%(95%CI 88.8%~99.9%),接受7~9个周期化疗的患者则分别为90.6%(95%CI 83.8%~98.1%)和85.4%(95%CI 78.3%~93.1%)。
最常见的3~4级不良事件是中性粒细胞减少症(187例)、贫血(82例)、腹泻(60例)、血小板减少症(46例)和低钾血症(35例),56例(12%)患者发生治疗相关的严重不良事件。3~4级不良事件以及2级或更严重神经病变的发生频率随着新辅助化疗周期数的增加而增加。研究没有报告治疗相关的死亡。
(编译 周阳)














